多替諾雷(Dotinurad,商品名:優(yōu)樂思)是一種新型促尿酸排泄藥����,由Fuji Yakuhin Co Ltd與衛(wèi)材共同研發(fā)。該藥物主要用于治療高尿酸血癥和痛風�����,已于2020年1月23日在日本獲批上市����。2024年1月22日,中國國家藥品監(jiān)督管理局藥品審評中心(CDE)受理了衛(wèi)材以5.1類新藥提交的多替諾雷片上市申請(NDA)�。
來源:國家藥審中心
作用機制
多替諾雷是一種高選擇性的尿酸鹽轉運蛋白1(URAT1)抑制劑����。它通過有效抑制腎近端小管URAT1的功能��,促進尿酸從腎臟排泄���,從而降低血尿酸水平����。與非選擇性URAT1抑制劑相比�,多替諾雷不影響尿酸排泄因子ABCG2和OAT1/3的功能,因此具有更高的降血尿酸效率���。
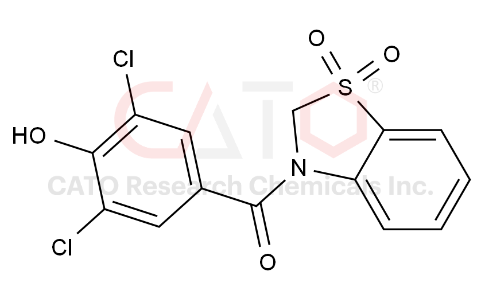
多替諾雷結構式
臨床研究
衛(wèi)材在中國開展了一項3期臨床研究(NCT05007392)�,旨在評估多替諾雷與非布司他治療痛風的療效��。該研究納入451例痛風患者���,隨機分為多替諾雷4 mg組和非布司他40 mg組�,主要研究終點是治療24周后血尿酸水平≤6.0 mg/dL的患者百分比�。
此前在日本進行的一項3期臨床研究結果顯示,多替諾雷4 mg治療伴或不伴痛風的高尿酸血癥患者����,在58周時血尿酸水平≤6 mg/dL的患者比例達到100%。長期使用對腎功能無明顯影響���,對肝功能也無臨床相關影響����。

URAT1作用機制
來源:TAKAHASHI CLINIC
臨床優(yōu)勢:
1. 高選擇性:多替諾雷選擇性抑制URAT1�,不影響其他尿酸轉運蛋白,提高了降血尿酸的效率��。
2. 高效性:相較于非選擇性URAT1抑制劑���,多替諾雷在相同治療時間內(nèi)可更有效地降低血尿酸水平��。
3. 安全性:多替諾雷的代謝產(chǎn)物不含有"對苯醌"或類似物��,可避免苯溴馬隆的肝毒性��。長期使用對腎功能和肝功能無明顯影響����。
4. 良好耐受性:臨床研究表明����,患者對多替諾雷的耐受性良好��。
專利情況
多替諾雷在中國擁有兩項核心專利:
1. 化合物專利(ZL201080042866.9):申請日為2010年9月29日�,理論到期日為2030年9月29日�����。
2. 晶型專利(ZL201880027057.7):申請日為2018年4月27日���,理論到期日為2038年4月27日�����,保護多替諾雷的II型結晶�。
值得注意的是�,晶型專利ZL201880027057.7目前面臨無效宣告請求,國家知識產(chǎn)權局于2024年4月30日發(fā)布了相關受理通知����。
市場前景
隨著生活水平的提高和飲食結構的變化,全球及中國的高尿酸血癥和痛風患病率呈上升趨勢��。根據(jù)弗若斯特沙利文的分析,預計到2025年��,全球痛風患者人數(shù)將達到2.7億�,到2030年將增至3.3億。在中國��,預計痛風患者人數(shù)在2025年將達到4,500萬�,2030年將達到5,200萬���。
全球痛風藥物市場規(guī)模預計將從2020年的26億美元增長至2025年的39億美元���,2023-2025年的年復合增長率估算為9.1%。在中國�����,盡管2021年受集采影響市場規(guī)模有所下滑�����,但網(wǎng)上藥店終端仍保持近30%的增長���,顯示出市場的韌性和潛力���。
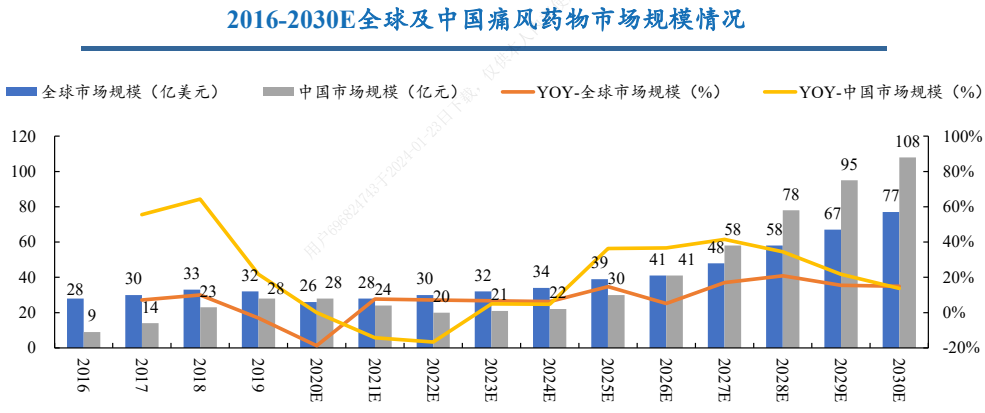
來源:Frost&Sullivan
競爭格局方面�,截至2023年12月�����,全球范圍內(nèi)臨床后期及已上市的高尿酸血癥及痛風性關節(jié)炎藥物共有147個���,其中URAT1是研發(fā)熱度最高的靶點����。多替諾雷作為新型URAT1選擇性抑制劑�,在這一快速增長的市場中具有顯著優(yōu)勢和潛力。
然而�����,多替諾雷也面臨一些挑戰(zhàn)���,如市場教育�、定價策略以及來自其他在研URAT1抑制劑的競爭壓力�����。盡管如此,考慮到其獨特的作用機制���、良好的安全性和顯著的臨床優(yōu)勢���,多替諾雷有望在這個快速增長的市場中占據(jù)重要地位,為眾多患者提供新的治療選擇�����。
為推動多替諾雷的研發(fā)進程��,CATO提供全套多替諾雷雜質(zhì)對照品��,助力藥物質(zhì)量控制和分析方法開發(fā)�����。
