格氏試劑
格氏試劑是格利雅試劑的簡稱��,以發(fā)現(xiàn)者V.A.Grginard名子命名��。性質(zhì)很活潑�����,易與水、二氧化碳�����、醇����、醛、酮�、酯、胺以及環(huán)氧化合物等反應�����,生成各種類型的有機化合物�,產(chǎn)率一般均較高,由鹵代烷與金屬鎂在無水乙醚溶劑中作用而制得�。通式為RMgX,R是烷基����、芳基或別的有機基,X是氯�、溴、碘���。例如CH3MgI����、C2H5MgBr和C6H5MgCl(Br)的醚溶液等�。格氏試劑是有機合成化學中的重要試劑,在元素有機化合物合成中也有廣泛應用���。使用時要嚴格防止與濕空氣接觸�,并注意著火的危險���。
【相關化學反應】
1����、格氏試劑可與各種不飽和鍵發(fā)生加成反應��,生成不同類型的產(chǎn)物����。反應時,格氏試劑中的C—Mg鍵斷裂�,烴基加到不飽和鍵中電子云密度小的原子上�,鎂原子加到電子云密度大的原子上�。
2、格氏試劑與二氯化鉛反應���,根據(jù)格氏試劑和二氯化鉛的用量不同�,可以生成二烴基鉛或四烴基鉛����。
3、格氏試劑與鹵化亞銅反應生成烴基亞銅.鹵化亞銅可以是碘化亞銅�����、溴化亞銅�����、氯化亞銅����。
4、格氏試劑與二鹵化汞反應生成烴基汞.常用的二鹵化汞是二溴化汞和二氯化汞.反應在乙醚等惰性溶劑中進行����。
5�、格氏試劑與等摩爾鹵化鋅反應��,生成烴基鹵化鋅����,格氏試劑過量則生成二烴基鋅�。常用的鹵化鋅是氯化鋅,常用的格氏試劑為C2H5MgXCH2=CHMgX�����,(CH3)3CMgX等���。
6�、格氏試劑與三鹵化硼反應�,生成烷基硼。格氏試劑中的鹵素可以是F��,Cl���, Br�����,I.三鹵化硼一般為BF3�,BCl3。產(chǎn)率為50%~90%.不能用這個反應制備三叔丁基硼��,因為叔丁基鹵化鎂與三氯化硼或三氟化硼作用時���,得到的是重排產(chǎn)物——叔丁基二異丁基硼或三異丁基硼��,機理不明����。
7�、格氏試劑與其它鹵代烴可以發(fā)生偶合作用,生成較高級的烴.常用的鹵代烴為溴代烴或碘代烴�����,氯代烴不夠活潑�����。反應式:R-MgX+X-R1===R-R1+MgX2��。
在此反應中�,金屬鹵化物是有效的催化劑�。R=R1時��,多用銀催化劑��,R≠R1時��,銅催化劑較為有效����。有乙烯基溴化物時可選用高鐵催化劑�����。若不活潑的乙烯基鹵化物或芳鹵可用二價鎳的二氯雙(三苯基膦)配合物或二氯化鈷催化�。二氯化鈷催化的反應歷程如下:
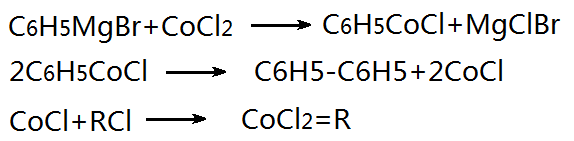
圖1為二氯化鈷催化的反應歷程。
【制備方法】
通常使金屬鎂與有機鹵代物在無水乙醚中反應而制得格氏試劑��。RX+Mg=RMgX
使用的原料和溶劑必須充分干燥�����。有機鹵代物可以是脂肪族或芳香族等��,根據(jù)鹵素的種類���、反應是否容易����,格利雅試劑收率高低而有所不同。反應的難易主要取決于鹵代烴中烴的結構和鹵素的種類��,若烴基相同�,碘最容易反應,氯最難反應��,但用碘時��,易發(fā)生Wutz副反應而降低收率�����。若鹵素相同���,烴基愈大�����,反應愈難��。有時為了提高收率�����,盡可能要低鹵濃度下及低溫度下反應���。為了提高反應速度�,在開始時加入少量碘來引發(fā)反應���,一旦反應開始�����,因為反應是放熱的,應迅速冷卻���。也可用少量1����,2-二溴乙烷代替碘�,特別是乙醚中有少量水時,采用此法更佳�����,因為生成的溴化鎂有脫水作用。關于溶劑��,可以采用乙醚�����、丁基醚��、四氫呋喃和苯甲醚等�。溶劑不同,直接影響反應的難易和收率的高低����,根據(jù)H.Normant的見解,以四氫呋喃較合適�,可使歷來感到困難的以氯乙烯、氯苯制取格氏試劑變得很容易���。這是因為氯乙烯與結合在烯碳上的氯不能在乙醚中與鎂反應����,但可在四氫呋喃中反應���,這樣制得的氯乙基鎂試劑�����,又稱為諾曼試劑�。除四氫呋喃外,也可用2-甲基四氫呋喃為溶劑��。在制取格利雅試劑時�����,若在二甲苯中進行���,反應速度很慢�����,滴加少量乙醚后,反應速度大大加快��,故可認為乙醚起著催化作用��。又經(jīng)證實�����,在加壓下氯烷和鎂作用,可直 接合成格利雅試劑����,而不需溶劑。利用間接的方法也可制得���,例如使溴乙基鎂與具有乙炔那樣的活潑氫化合物作用�����,可產(chǎn)生金屬與氫的置換反應���,從而制得溴乙炔基鎂?;蛘吲c溴化鎂反應,置換金屬��,如下圖2:
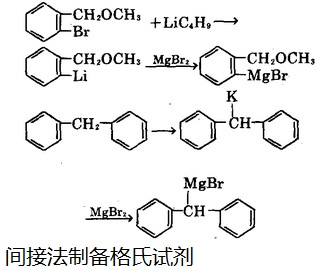
圖2為間接法制備格氏試劑�����。