截至2025年4月3日�����,美國疾病控制與預(yù)防中心(CDC)報告稱����,全美已有22個州共報告607例麻疹確診病例�����,其中得克薩斯州最為嚴重���,累計達400例�����,并出現(xiàn)2例死亡�����?�?八_斯州與俄克拉荷馬州等地也相繼爆發(fā)疫情�����,病例持續(xù)上升��。
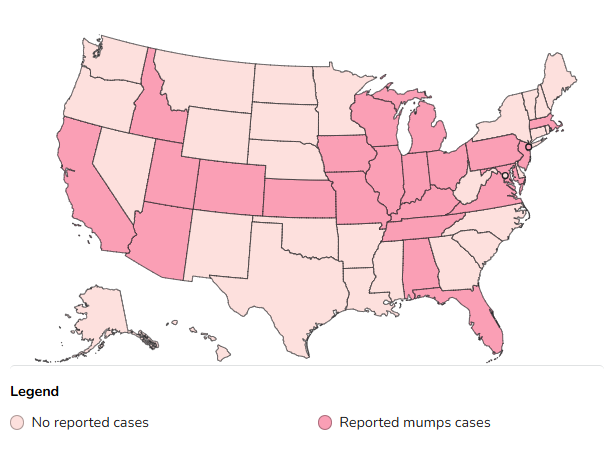
Fig.1.Reported U.S. mumps cases by jurisdiction, 2025.(from CDC)
這場疫情不僅刷新了2024年的全年紀錄��,更暴露出接種率下降的嚴重后果����。而作為一種早已可通過疫苗控制的傳染病��,麻疹為何仍能卷土重來�?本文將帶你回到病毒本身,重新認識它的傳播機制�、疫苗發(fā)展歷程,并探討一個鮮為人知的研究前沿:麻疹病毒���,或許還能被用于抗癌治療�����。
麻疹病毒為何“如此難防”
麻疹病毒(Measles virus, MeV)是一種典型的高傳染性病毒����,屬于副黏液病毒科(Paramyxoviridae)、麻疹病毒屬(Morbillivirus)�����,為一種具有包膜的單股負鏈RNA病毒�����。病毒顆粒呈球形����,直徑約為120–250 nm,外層包裹脂質(zhì)雙層膜�,表面存在兩種重要的刺突糖蛋白:血凝素(Hemagglutinin, H)和融合蛋白(Fusion protein, F),是病毒識別并進入宿主細胞的關(guān)鍵分子�����。
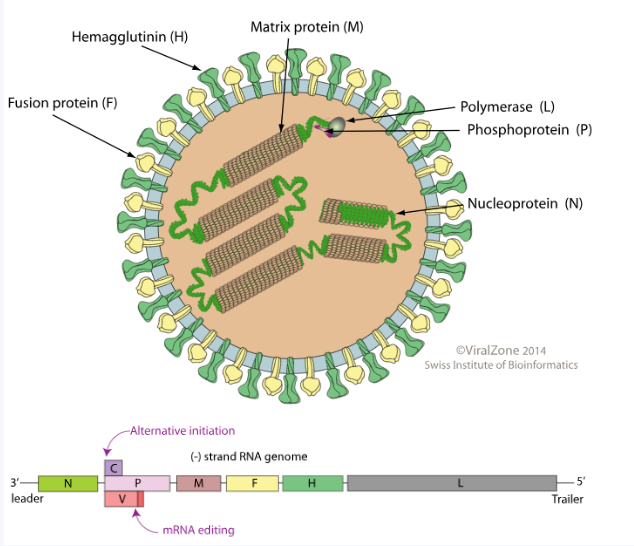
Fig.2. 麻疹病毒結(jié)構(gòu)示意圖
麻疹病毒基因組全長約15.9 kb���,編碼六個主要結(jié)構(gòu)基因:N�、P、M��、F���、H、L���,其中P基因通過RNA編輯機制可翻譯出多個蛋白���,共計可表達八種功能蛋白。這些蛋白協(xié)同完成病毒的復(fù)制���、組裝與傳播��,具體功能如下:
核蛋白(Nucleoprotein):緊密包裹病毒RNA���,形成核衣殼(nucleocapsid),在病毒復(fù)制和轉(zhuǎn)錄過程中起到模板保護和穩(wěn)定作用�����。
磷蛋白(Phosphoprotein):與L蛋白共同構(gòu)成RNA依賴的RNA聚合酶復(fù)合體(RdRp),參與病毒RNA的復(fù)制與mRNA轉(zhuǎn)錄��。此外��,P基因還能通過RNA編輯表達出V�����、C等調(diào)節(jié)蛋白����,在病毒復(fù)制調(diào)控和免疫逃逸中發(fā)揮作用。
基質(zhì)蛋白(Matrix protein):定位于病毒包膜內(nèi)側(cè)��,是病毒組裝與出芽的重要結(jié)構(gòu)蛋白����,維持病毒粒子的結(jié)構(gòu)完整性。
融合蛋白(Fusion protein):介導(dǎo)病毒包膜與宿主細胞膜的融合�,是病毒進入宿主細胞必不可少的因子,同時也是疫苗設(shè)計和中和抗體研究的重要靶點��。
血凝素蛋白(Hemagglutinin):負責(zé)識別宿主細胞表面受體���,包括CD150(SLAMF1)和Nectin-4����,起始病毒吸附過程,是決定病毒宿主范圍和組織嗜性的關(guān)鍵因子�����。
大蛋白(Large protein):為RNA聚合酶的催化亞基�����,具備多種酶活性�,負責(zé)病毒基因組的轉(zhuǎn)錄與復(fù)制全過程��。
上述這些結(jié)構(gòu)特征使得麻疹病毒在感染細胞��、擴散�����、逃避免疫等方面具備“高效執(zhí)行力”�。
麻疹疫苗簡史:從病毒株研發(fā)到防疫困境
截止目前,麻疹疫苗仍是預(yù)防麻疹最有效��、最經(jīng)濟的公共衛(wèi)生工具��,它的誕生是20世紀公共衛(wèi)生史上的重要轉(zhuǎn)折。1954年����,科學(xué)家Edmonston首次分離出麻疹病毒株,并通過連續(xù)傳代減毒���,最終于1963年開發(fā)出減毒活疫苗�����。1968年����,副作用更低�、保護率更高的Edmonston-Enders株成為全球標準毒株,并被廣泛用于MMR疫苗(麻疹-腮腺炎-風(fēng)疹三聯(lián)疫苗)的生產(chǎn)�。
除了減毒活疫苗,近年來的研究也探索了其他疫苗形式�,如:
mRNA疫苗平臺:使用 LNP-mRNA 麻疹疫苗來預(yù)防致命的麻疹病毒感染;
單劑量口腔崩解膜(ODF):利于偏遠地區(qū)接種�;
通用兒童聯(lián)合疫苗:將多種兒科疫苗整合至同一制劑中。
麻疹疫苗可提供超過97%的保護���,自1960年代推廣以來已顯著降低全球發(fā)病率和死亡率����,挽救逾3000萬生命。本次疫情的核心問題并非疫苗效力��,而在于接種率下滑�����。目前麻疹病毒的基本傳染數(shù)(R?)高達12–18���,需95%以上的群體接種率才能建立有效免疫屏障���。近年來�,疫苗猶豫、虛假信息傳播以及資源不均等問題導(dǎo)致部分地區(qū)接種率低于90%�����,為病毒傳播提供可乘之機����,最終引發(fā)2025年的局部流行。
病毒的另一面:它或許還能對抗癌癥
雖然麻疹病毒在公共衛(wèi)生領(lǐng)域被視為“高危病原體”,但研究人員正努力揭示它的另一面�����。在多個實驗中�,減毒麻疹病毒株(如Edmonston株)表現(xiàn)出對腫瘤細胞的天然親和性,具備成為溶瘤病毒的潛力�����。這種“病毒反轉(zhuǎn)身份”的探索�,為癌癥治療打開了新的研究方向。
麻疹病毒介導(dǎo)的腫瘤溶解機制
發(fā)表于《Viruses》期刊的綜述 Measles to the Rescue: A Review of Oncolytic Measles Virus(2016)指出�,麻疹病毒可通過多種機制實現(xiàn)腫瘤細胞殺傷:

Fig.3. Measles to the Rescue: A Review of Oncolytic Measles Virus(Viruses. 2016 Oct 22;8(10):294. doi: 10.3390/v8100294)
靶向感染:通過識別CD46與Nectin-4等腫瘤相關(guān)受體實現(xiàn)選擇性入侵;
細胞融合裂解:感染后誘導(dǎo)腫瘤細胞融合形成多核巨細胞(syncytia)���,引發(fā)裂解性細胞死亡����;
激活免疫系統(tǒng):激發(fā)樹突狀細胞成熟與CD8? T細胞浸潤�,增強抗腫瘤免疫反應(yīng);
可編程病毒載體:基因工程手段可為麻疹病毒引入NIS�、免疫調(diào)節(jié)因子、腫瘤靶向配體等���,以提升靶向性與治療效率�。
目前,工程化麻疹病毒已進入卵巢癌�、膠質(zhì)母細胞瘤和多發(fā)性骨髓瘤等多種癌癥的I期臨床試驗階段,展現(xiàn)出良好的安全性和初步療效��。
重新認識病毒��,也是在重新定義人類與疾病的關(guān)系
麻疹病毒仍是當(dāng)今公共衛(wèi)生的一大挑戰(zhàn)��,尤其在接種率下降的背景下�����,其傳播風(fēng)險不容低估���。然而����,從“致病因子”到“抗癌工具”的身份轉(zhuǎn)變����,也說明了科學(xué)在改變?nèi)祟惻c病毒關(guān)系中的力量�。防控疫情�,離不開對疫苗的信任與普及�;探索治療,也依賴于對病毒機制的深入理解���。在未來�����,我們或許會同時在疫苗接種門診與腫瘤治療病房中����,看見這個古老病毒的新角色��。
abinScience相關(guān)產(chǎn)品推薦
作為法國 ProteoGenix 旗下的重要品牌����,abinScience 專注于生物試劑的研發(fā)與生產(chǎn),致力于為全球科研人員提供高質(zhì)量�����、創(chuàng)新型的研究工具與技術(shù)方案��。依托 ProteoGenix 的研發(fā)平臺與嚴格質(zhì)控��,abinScience 構(gòu)建了覆蓋 蛋白與抗體十余大類的核心產(chǎn)品線,包括傳統(tǒng)多抗��、內(nèi)參抗體�、標簽抗體、高活性重組蛋白���、in vivo 功能性抗體����、流式抗體��、納米抗體�����、磷酸化抗體��、DNA/RNA 抗體��、PEG 抗體與特色小分子抗體等����。abinScience 在自身免疫��、病毒與細菌、神經(jīng)科學(xué)��、免疫靶點等研究方向建立了完整產(chǎn)品矩陣�,涵蓋抗體、重組蛋白�����、檢測試劑盒與功能研究工具�。高靈敏度、高特異性是我們始終堅持的標準��,為全球生命科學(xué)基礎(chǔ)研究提供跨學(xué)科�����、多維度的研究支持����。
以下是abinScience提供的麻疹病毒相關(guān)的蛋白、抗體產(chǎn)品清單���,更多產(chǎn)品可掃碼聯(lián)系專員咨詢����!

??Proteins:
Recombinant MeV H/Hemagglutinin glycoprotein Protein, C-His
Recombinant MeV H/Hemagglutinin glycoprotein Protein, N-His
Recombinant MeV F1/Fusion glycoprotein F1 Protein, N-His
Recombinant MeV N/Nucleoprotein Protein, N-His
Recombinant MeV M/Matrix protein Protein, N-His
Recombinant MeV P/Phosphoprotein Protein, N-His
Recombinant MeV V/Non-structural protein V Protein, N-His
Recombinant MeV C/Protein C Protein, N-His
Recombinant MeV F/Fusion Protein, C-Strep
Recombinant MeV H/Hemagglutinin Protein, C-Strep
??Antibodies:
Anti-MeV M/Matrix Polyclonal Antibody
Anti-Mev F/Fusion Antibody (mAb 77)
Anti-Mev F/Fusion Antibody (mAb 77)
參考文獻:
1. Blechacz B, Russell SJ. Measles virus as an oncolytic vector platform. Curr Gene Ther. 2008;8(3):162-175. doi:10.2174/156652308784746459IF: 3.8 Q2
2. Noyce RS, Bondre DG, Ha MN, et al. Tumor cell marker PVRL4 (nectin 4) is an epithelial cell receptor for measles virus. PLoS Pathog. 2011;7(8):e1002240. doi:10.1371/journal.ppat.1002240
3.Aref, Sarah et al. “Measles to the Rescue: A Review of Oncolytic Measles Virus.” Viruses vol. 8,10 294. 22 Oct. 2016, doi:10.3390/v8100294