在生命科學(xué)的探索征程中��,優(yōu)質(zhì)的科研試劑宛如開啟未知之門的鑰匙����。每一位投身生命科學(xué)研究的小伙伴,都懷揣著對未知的熱忱與執(zhí)著���。AntibodySystem陪伴各位小伙伴走過漫漫科研長路��,并為大家提供有力支持�。
在2025年3月�����,AntibodySystem又見證了無數(shù)科研人的拼搏與突破�����。今天就來和大家分享一下本月引用AntibodySystem產(chǎn)品的部分文獻(xiàn)�����,和Connie一起交流學(xué)習(xí)�����,共同進(jìn)步�!
One



Targeting the ceramidase ACER3 attenuates cholestasis in mice by mitigating bile acid overload via unsaturated ceramide-mediated LXRβ signaling transduction
Nat Commun. 2025 Mar 2;16(1):2112.
Recombinant Human NR1H2/LXRb Protein, N-His
文獻(xiàn)重點(diǎn)內(nèi)容總結(jié)
膽汁酸過載是膽汁淤積性肝損傷(CLI)的核心致病機(jī)制,該研究揭示堿性神經(jīng)酰胺酶(ACER3)在CLI中通過調(diào)控神經(jīng)酰胺CER(d18:1/18:1)-LXRβ信號軸發(fā)揮關(guān)鍵作用�����。CLI中ACER3表達(dá)顯著上調(diào)�,且與患者CLI嚴(yán)重程度呈正相關(guān)。機(jī)制層面�,CER (d18:1/18:1)直接結(jié)合肝臟X受體β(LXRβ)配體結(jié)合域,作為激動劑激活其轉(zhuǎn)錄功能���,緩解肝細(xì)胞膽汁酸過載���。研究揭示了CER-LXRβ互作在膽汁酸穩(wěn)態(tài)中的新機(jī)制,為CLI治療提供靶點(diǎn)�����。
Recombinant Human NR1H2/LXRb Protein, N-His的應(yīng)用及實(shí)驗(yàn)結(jié)果
在驗(yàn)證CER (d18:1/18:1)與LXRβ直接結(jié)合的實(shí)驗(yàn)中����,作者采用表面等離子體共振(SPR)技術(shù)�����,將不同濃度(0�����、125���、250、500���、1000nM)的Recombinant Human NR1H2/LXRb Protein, N-His(購自AntibodySystem�,貨號:YHF08201)溶解于PBS后注入固定有CER(d18:1/18:1)的芯片�����。
結(jié)果顯示���,LXRβ與CER (d18:1/18:1)呈劑量依賴性結(jié)合���,結(jié)合親和力通過SPR信號響應(yīng)值定量分析確認(rèn)。此外�,免疫共沉淀(Co-IP)實(shí)驗(yàn)進(jìn)一步證實(shí)了CER (d18:1/18:1)與LXRβ的物理相互作用,且分子對接模擬表明CER(d18:1/18:1)優(yōu)先結(jié)合LXRβ配體結(jié)合域的關(guān)鍵氨基酸殘基(如His433和Trp457)�����。這些結(jié)果直接支持了CER (d18:1/18:1)作為LXRβ內(nèi)源性配體的功能���,并解釋了其通過激活LXRβ信號通路調(diào)控膽汁酸代謝和脂質(zhì)穩(wěn)態(tài)的分子機(jī)制����,為靶向ACER3-CER-LXRβ軸治療CLI提供了實(shí)驗(yàn)依據(jù)����。

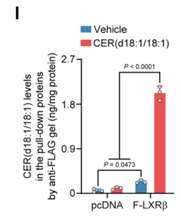
圖8j. SPR滴定曲線反映了重組人LXRβ與CER(d18:1/18:1)之間的相互作用
圖8k. Flag-LXRβ的Co-IP
圖8l. CER(d18:1/18:1)在免疫共沉淀LXRβ-FLAG蛋白中表達(dá)
Two


文獻(xiàn)重點(diǎn)內(nèi)容總結(jié):
RBM39作為剪接體的核心組分,在維持mRNA完整性中發(fā)揮關(guān)鍵作用�。其缺失可顯著加劇RNA剪接缺陷并展現(xiàn)出強(qiáng)效抗癌活性。多組學(xué)分析比較降解劑CB039與Indisulam揭示CEP192是RBM39缺失的核心下游靶點(diǎn)�����,96%癌細(xì)胞系依賴其功能��。在癌細(xì)胞模型中��,兩種降解劑均誘導(dǎo)CEP192外顯子42跳躍并降低其蛋白水平。機(jī)制研究表明�,CB039處理或RNA干擾介導(dǎo)的CEP192敲低可導(dǎo)致紡錘體紊亂、染色體異常及G2/M期阻滯�����。研究首次確立CEP192為RBM39降解劑的核心效應(yīng)蛋白��,為抗癌藥物研發(fā)提供新方向�����。
Recombinant Human RBM39 Protein, N-His的應(yīng)用及實(shí)驗(yàn)結(jié)果:
本研究通過熒光偏振(FP)實(shí)驗(yàn)驗(yàn)證了CB039對RBM39-DCAF15-DDB1三元復(fù)合物的調(diào)控作用����。作者使用Recombinant Human RBM39 Protein(購自AntibodySystem,貨號:YHF08201)與DCAF15-DDB1復(fù)合物及熒光探針Probe-3共同孵育�����。

圖F. 用于評估DCAF15-DDB1�、RBM39ru.v26與Probe-3形成三元復(fù)合物的FP實(shí)驗(yàn)示意圖
結(jié)果顯示,在RBM39存在時(shí)����,DCAF15-DDB1與Probe-3的結(jié)合IC50值為208 nM�,而單獨(dú)DCAF15-DDB1或RBM39的親和力顯著降低(IC50 > 2000 nM)���,證實(shí)了RBM39作為“分子膠”對復(fù)合物形成的必要性�����。
競爭性FP實(shí)驗(yàn)進(jìn)一步表明,CB039和Indisulam可劑量依賴性地置換Probe-3�,IC50分別為594 nM和417 nM,提示CB039與靶點(diǎn)的結(jié)合模式與Indisulam類似但存在差異�。
該實(shí)驗(yàn)體系為定量評估RBM39降解劑的結(jié)合效率及機(jī)制提供了關(guān)鍵工具,并支持了CB039通過增強(qiáng)RBM39與DCAF15相互作用發(fā)揮降解活性的結(jié)論���。
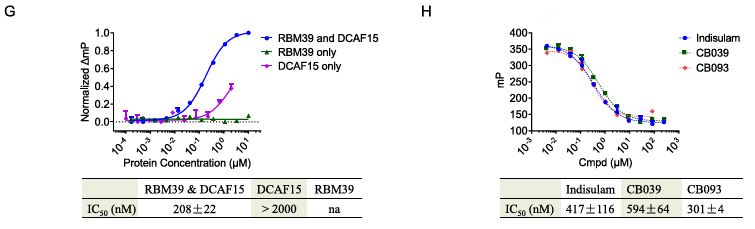
圖2G. FP結(jié)合實(shí)驗(yàn)
圖2H. 競爭性FP滴定實(shí)驗(yàn)
Three


TSHR-targeting nucleic acid aptamer treats Graves' ophthalmopathy via novel allosteric inhibition
bioRxiv 2025.03.07.641992
Research Grade Teprotumumab
文獻(xiàn)重點(diǎn)內(nèi)容總結(jié)
該研究開發(fā)了一種名為YC3的核酸適配體��,通過靶向促甲狀腺激素受體(Thyroid stimulating Hormone Receptor�����,TSHR)治療Graves眼?��。?/span>Graves’ ophthalmopathy,GO)���。TSHR信號通路的異常激活是GO等疾病的核心機(jī)制��,但目前尚無臨床可用的TSHR抑制劑�����。作者采用創(chuàng)新性的“蛋白靶向細(xì)胞-SELEX”結(jié)合功能篩選策略�����,成功篩選出具有納摩爾級親和力的YC3�。研究首次為TSHR變構(gòu)抑制治療GO提供了臨床前證據(jù),并揭示了TSHR的新型藥物靶點(diǎn)�����,為開發(fā)精準(zhǔn)療法奠定了基礎(chǔ)�����。
Research Grade Teprotumumab的應(yīng)用及實(shí)驗(yàn)結(jié)果
本研究使用Research Grade Teprotumumab(購自AntibodySystem���,貨號:DHC29903)作為陽性對照藥物用于評估YC3的療效�。
實(shí)驗(yàn)中,Teprotumumab(5μg/mL)與YC3(2μM)在抑制GOFs的炎癥因子(IL-6���、IL-8�、IL-1β)分泌和透明質(zhì)酸合成酶(HAS1-3)表達(dá)方面表現(xiàn)出相似效果���,且兩者均能顯著減少細(xì)胞外基質(zhì)(ECM)沉積�����。
此外,在GO小鼠模型中�,Teprotumumab與YC3均能緩解眼眶組織炎癥浸潤和纖維化,改善甲狀腺功能亢進(jìn)癥狀�����。研究還提出未來可探索YC3與Teprotumumab聯(lián)用的多靶點(diǎn)治療策略�����,以進(jìn)一步提升GO治療效果��。Teprotumumab的引入不僅驗(yàn)證了YC3的潛在臨床價(jià)值��,也為適配體藥物的開發(fā)提供了療效對比的基準(zhǔn)。
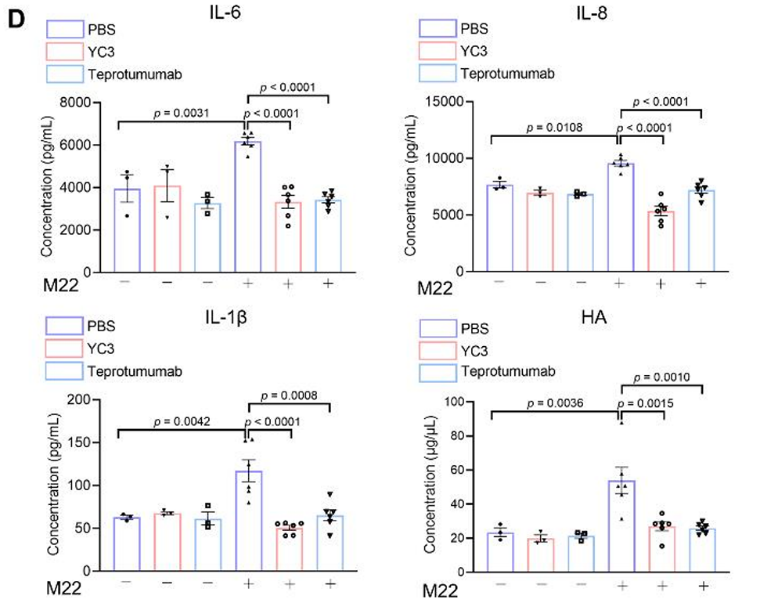
圖6D. ELISA檢測M22刺激的GO患者GOFs細(xì)胞上清中IL-6�、IL-8、IL-1β及HA水平����,細(xì)胞經(jīng)YC3適配體(2 μM)或Teprotumumab(5 μg/mL)處理
以上為2025年3月部分引用AntibodySystem產(chǎn)品的科研文獻(xiàn)。AntibodySystem可提供覆蓋重組蛋白����、流式抗體、抗IgE抗體�����、磷酸化抗體��、ELISA試劑盒等全系列科研試劑產(chǎn)品���,精準(zhǔn)服務(wù)于藥物靶點(diǎn)研究����、免疫分析�、過敏機(jī)制探索及腫瘤治療開發(fā)等領(lǐng)域。
同時(shí)為了感謝廣大科研工作者對AntibodySystem SAS的支持與信任����,佰樂博和AntibodySystem SAS聯(lián)合推出2025年度文獻(xiàn)引用獎(jiǎng)勵(lì)活動��。凡在SCI期刊上發(fā)表文章并使用AntibodySystem SAS全線產(chǎn)品的科研工作者�����,均可申請獎(jiǎng)勵(lì)�����,具體活動詳情可至佰樂博官網(wǎng)或微信公眾號了解��。
